符号计算改良的分析化学计算方法
摘要
两性物质 NaHA 溶液的 PH 计算是分析化学的重要内容。教科书介绍了多种 PH 近似公式,但各公式的适用条件一度缺少详细论证,且目前仍然处于争论之中。本文以 Mathematica 符号计算软件为辅助,发扬了分析化学去公式化计算方法。针对学术界一直头疼的NaHA 酸碱度计算公式的选择问题,作者利用数学分析方法及可视化手段,深刻揭示了各公式的可行域空间,力求为分析化学师生彻底扫除障碍。
引言
二元弱酸 H2A 的酸式盐 NaHA 为两性物质。在浓度为 c 的 NaHA 溶液中有以下关系:
- 电荷守恒: [Na+]+[H+]=[HA−]+2[A2−]+[OH−]
- 物料守恒: [Na+]=[H2A]+[HA−]+[A2−]
- 一级电离: K1=[H2A][H+][HA−]
- 二级电离: K2=[HA−][H+][A2−]
为了简化计算,引入分析浓度 c(A的总浓度)与分布分数(组分占有 c 的比例):
[H2A][HA−][A2−]=c∗[H+]2+[H+]K1+K1K2[H+]2=c∗[H+]2+[H+]K1+K1K2[H+]K1=c∗[H+]2+[H+]K1+K1K2K1K2
将上述组分浓度代入电荷守恒,得到关于氢离子浓度[H+]的高次多项式方程:
c+[H+]=[H+]2+[H+]K1+K1K2[H+]K1+2K1K2+[H+]Kw
其中 Kw 为水的离子积常数,此处默认常温下 Kw=10−14 。对于给定的二元酸式盐 NaHA ,已知两级电离常数 K1 和 K2 ,给定浓度 c ,求解上述方程即可得知此时氢离子浓度的准确值(忽略离子活度)。但由于上述方程求解不便,传统分析化学的处理方法为引入近似条件,将氢离子浓度[H+]化简为显函数形式。以下是经典教科书中给出的四个近似公式及其适用条件:
[Hx1][Hx2][Hx3][Hx4]=c+K1K1(c∗K2+Kw)=c+K1K1(c∗K2)=K1K2=cK1(c∗K2+Kw)cccc≥500K2≥500K2&&K2c≥20Kw≥20K1≥500K2&&K2c≥20Kw
传统体系“记忆换运算,近似换简化”的思路同学们都不陌生。然而,这样的近似公式会造成学习上的不便甚至混淆:
- 一些公式的适用范围存在交集,实际应用中究竟哪一个公式适用区间更普遍?
- 适用的边界条件究竟如何与 物理意义(二级电离、水的电离)相联系?
在计算机高度发达的今天,我们可以很轻易地求解高次多项式方程,传统近似手段简化运算的价值正逐渐丧失。并且,如何真正完备地刻画使用公式带来的误差以及它们的适用范围,成为目前去公式化方法和传统体系之间的主要矛盾。为此,本文以 Mathematica 为平台,充分运用数学、计算机手段,讨论近似公式的可行域区间,推动分析化学课程的发展。
数学准备
可行域
由于 [H+]、K1、K2,c 数值非常小,对它们取负对数之后, PH、PK1、PK2、Pc 四个变量满足的关系如下:
PH1PH2PH3PH4=−log1010−Pc+10−PK110−PK1(10−Pc∗10−PK2+Kw)=−log1010−Pc+10−PK110−PK1(10−Pc∗10−PK2)=−log1010−PK1∗10−PK2=−log1010−Pc10−PK1(c∗10−PK2+Kw)
引入相空间 R3={x=(PK1,PK2,Pc)∣PK1,PK2,Pc∈R} 以描述已知的三个初始条件。如此一来,四大公式可看作 R3→R,(x→PH) 一个映射。
我们的目的,在于找出所有满足“相对准确值误差在5%以内”的三维点所构成的集合。由函数的连续性可知,它是一个连通集。以相对氢离子准确值误差 5%为标准,设 PH 准确值为 F(x),x=(PK1,PK2,Pc) ,定义误差函数 Δ(x),x∈R3。简单推导可知,Δ(x)=∣fi(x)−F(x)∣≤0.02即为所求区域满足的限制条件。我们称不等式的解集为可行域。
对数变换
将这一对应关系写作:
f1(PK1,PK2,Pc)f2(PK1,PK2,Pc)f3(PK1,PK2,Pc)f4(PK1,PK2,Pc)=−log1010−Pc+10−PK110−PK1(10−Pc∗10−PK2+Kw)=−log1010−Pc+10−PK110−PK1(10−Pc∗10−PK2)=−log1010−PK1∗10−PK2=−log1010−Pc10−PK1(10−Pc∗10−PK2+Kw)
由数学分析知识可知,所有满足条件的点,在相空间中分布于边界曲面的同一侧。对原方程作对数变换:
10−Pc+10−PH=10−2PH+10−PH10−PK1+10−PK110−PK210−PH10−PK1+2∗10−PK110−PK2+10−PHKw
几乎无法表示为PH关于PK1、PH2、Pc 的显函数,误差函数 Δ(x) 难于推导。故退而寻求数值解。
线性近似公式的解析与讨论
作图
公式 [Hx3] 经对数变换后的形式较为简单——$PH $关于 PK1 和 PK2具有线性性质,在新的相空间 R3={y=(PK1,PK2,PH)∣PK1,PK2,PH∈R}中的图像是一张平面:
PH=21PK1+21PK2
在相空间 R3={y=(PK1,PK2,PH)∣PK1,PK2,PH∈R}中,满足与精确酸度方程误差0.02 的两张曲面分别是:
10−Pc+10−(PH−0.02)10−Pc+10−(PH+0.02)=10−2(PH−0.02)+10−(PH−0.02)10−PK1+10−PK110−PK210−(PH−0.02)10−PK1+2∗10−PK110−PK2+10−(PH−0.02)Kw=10−2(PH+0.02)+10−(PH+0.02)10−PK1+10−PK110−PK210−(PH+0.02)10−PK1+2∗10−PK110−PK2+10−(PH+0.02)Kw
与PH=21PK1+21PK2联立消去 PH,即得 R3中关于 (PK1,PK2,Pc)的方程
10−Pc+10−(21PK1+21PK2−0.02)10−Pc+10−(21PK1+21PK2+0.02)=10−2(21PK1+21PK2−0.02)+10−(21PK1+21PK2−0.02)10−PK1+10−PK110−PK210−(21PK1+21PK2−0.02)10−PK1+2∗10−PK110−PK2+10−(21PK1+21PK2−0.02)Kw=10−2(21PK1+21PK2+0.02)+10−(21PK1+21PK2+0.02)10−PK1+10−PK110−PK210−(21PK1+21PK2+0.02)10−PK1+2∗10−PK110−PK2+10−(21PK1+21PK2+0.02)Kw
对应的曲面即是可行域的边界。分别记作 sup(x) 和 inf(x),作图如下:
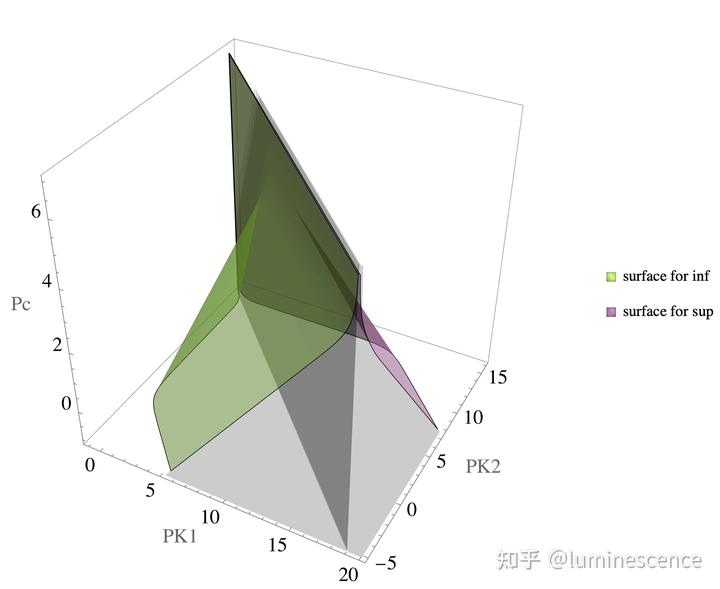
可行域就是图中的阴影区域。
讨论
公式 f3 的秘密已经一览无余。比如固定 Pc=2,误差函数
Δ(PK1,PK2,2)=∣f3(PK1,PK2,2)−F(PK1,PK2,2)∣
的解为 R2 的子集,是可行域在 Pc=2 处的截面:
又如,对公式的适用条件
c≥500K2c≥500K2&&K2c≥20Kwc≥20K1condition1condition2condition3
作对数变换得
PcPc+PK2Pc≤log(500)PK2≤log(20)Kw≤log(20)PK1condition1condition2condition3
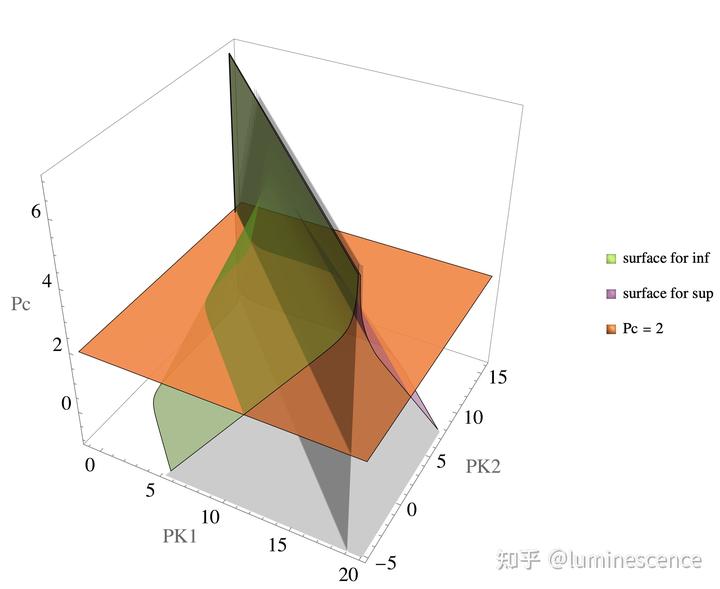
可见变换后的结果都描述了相空间 R3={x=(PK1,PK2,Pc)∣PK1,PK2,Pc∈R} 中一个以平面为边界的区域。将它们和完整的可行域放在一起考虑:
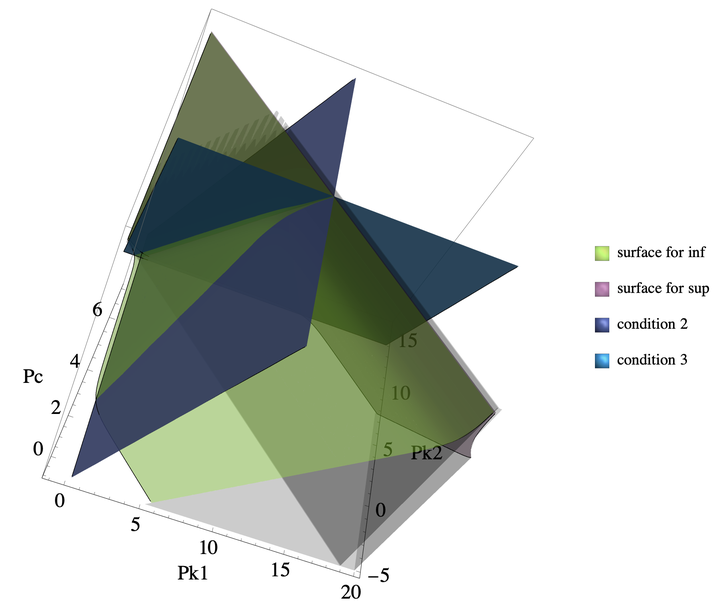
可见这些限制都具有一定的局限性。现今对于传统条件中 20 、 500 等位置的常数更准确的研究即可简化为:寻找可行域边界曲面的最优二元线性拟合函数——在本文提出完整可行域之后便可迎刃而解。在此,作者建议用 10.365来替代条件 Pc+PK2≥log(20)Kw 中原本“ 20 ”的位置。
代码附于文末,读者可自行尝试。
其他公式
其他可行域
不难从以上步骤总结出研究计算可行域的一般方法:对数变换 ⇒ 刻画误差 ⇒ 消去 PH ⇒ 作图。如法炮制,易得四大公式可行域的边界如下:
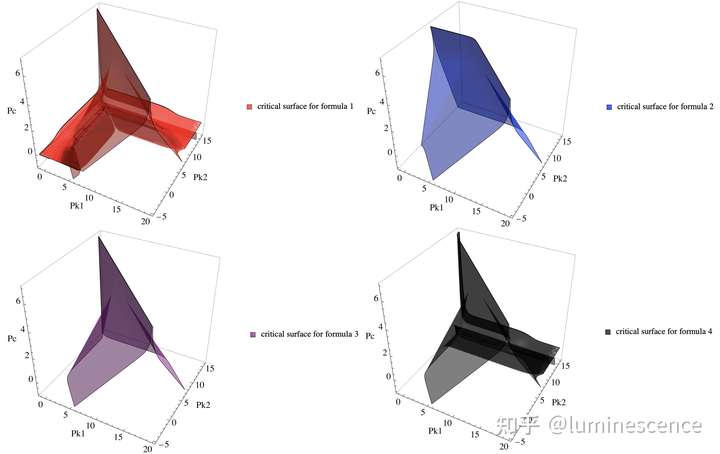
结合公式 f3 的经验以及可行域的实际物理意义,读者不难判断可行域的位置。可以发现,在分析浓度小于 10−6的区间,所有近似公式基本完全失效。
最优近似
由于计算能力的不足,前人对于“哪一个公式在给定误差下的可行域最广?”的问题难以给出明确的回答。然而在计算系统高度发达的当下,找出这一最优公式已是易如反掌。我们借助可视化手段,将四大公式的可行域边界分别重叠:
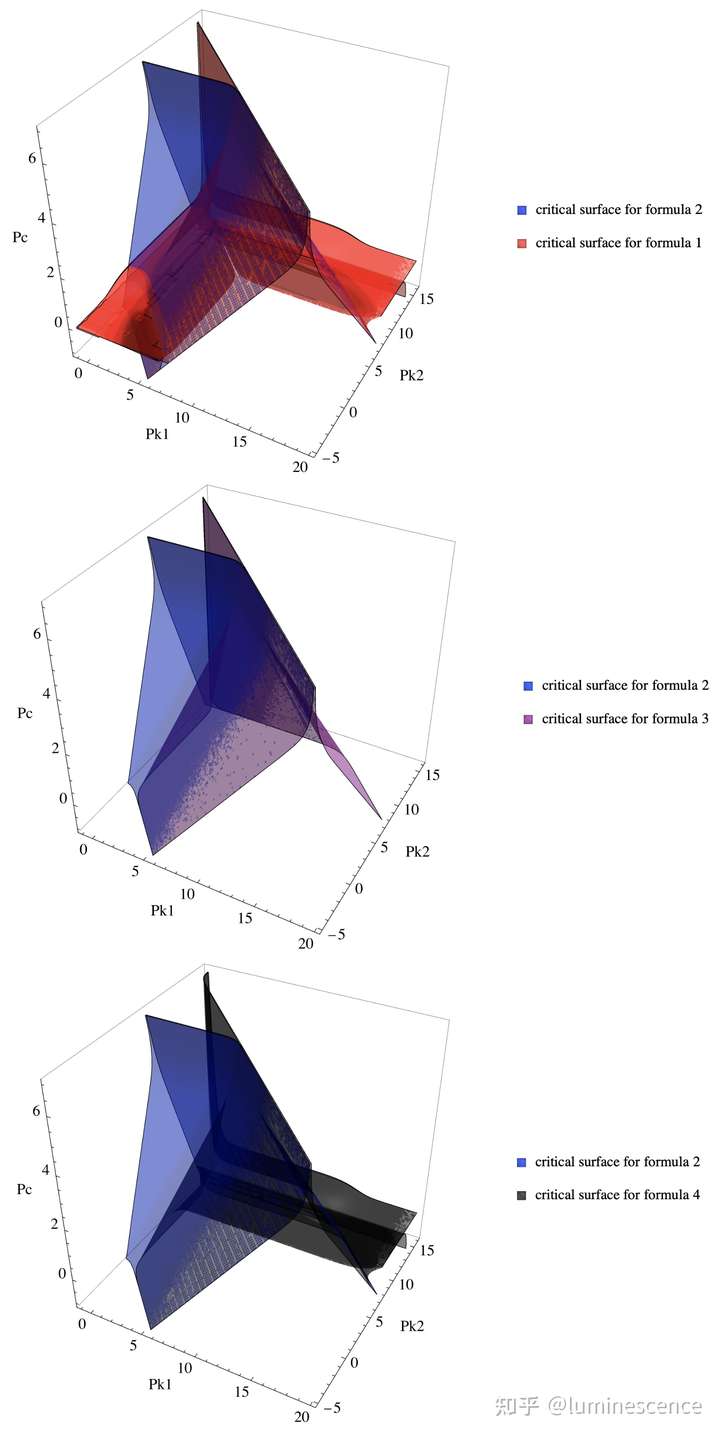
可见公式
[H]x2=c+K1K1(c∗K2)
对应的可行域最为宽广。在误差不大于 5% 的标准下的优越性一目了然。
结论
本文以相对精确结果 [H+] 偏差 5% 为标准,使用数学方法和计算机手段,引入描述已知条件的 R3相空间,深刻揭示了 NaHA 酸碱度四大近似公式的可行域。希望能为分析化学师生彻底扫除认知障碍。
对于具体公式的选择问题上,基于可行域空间最宽广的原则,公式
[H]=c+K1K1(c∗K2)
是其中最优。虽然其他公式有一定的物理意义,但实际效果并不大,剔除之无大碍。
对于形如 NamHnA 的更多元酸式盐,已知条件是 m+n+1维向量 $ (PK_1\dots,PK_n,Pc)$,可行域的边界曲面将在高维空间中展开。本文的方法虽然在原则上仍然适用,但略显复杂,需要更多的线性代数知识来辅助处理。如果过程过于复杂,可以参考 EDTA 配位滴定金属离子的处理方式,引入“表观浓度”以简化运算。
交流电和生物电是两种不同的资源,它们应当各得其所。用计算机手段求解化学平衡问题,一定是分析化学课程教学改革的发展方向。
鸣谢
本文写作得到了中国科学技术大学化学系邵利民副教授的鼎力支持。
面对一些困难,刘毅凡同学为作者提供了很多帮助和鼓励。
此外还有来自四面八方的建议,在此一并感谢!
部分代码
c=0.1下的精确PH:
c = 0.1;
accurate =
ContourPlot3D[
c + 10^-PH == kw/10^-PH + c ((10^-PH*10^-Pk1 + 2*10^-Pk1*10^-Pk2)/
(10^(-2 PH) + 10^-PH*10^-Pk1 + 10^-Pk1*10^-Pk2)), {Pk1, 0, 20},
{Pk2, 0, 20}, {PH, 0, 14},PlotTheme -> "Scientific", AxesLabel ->
Automatic, AxesStyle -> Directive[14], PlotLegends -> {"accurate PH"},
PlotRange -> Full]
|
特定浓度可行域:
c = 0.1;
cp3sup =
Table[{FindRoot[{c + 10^-(PH - 0.02) ==
kw/10^-(PH - 0.02) + c ((10^-(PH - 0.02)*10^-Pk1 + 2*10^-Pk1*10^-Pk2)/(
10^(-2 (PH - 0.02)) + 10^-(PH - 0.02)*10^-Pk1 + 10^-Pk1*10^-Pk2)),
PH == 1/2 Pk1 + 1/2 Pk2, Pk2 == a}, {Pk1, 20}, {Pk2, a}, {PH, 20},
WorkingPrecision -> MachinePrecision][[1, 2]], a}, {a, 0, 14, 0.05}];
cp3supline =
ListLinePlot[cp3sup, PlotTheme -> "Detailed", PlotStyle -> Orange,
FrameLabel -> {{HoldForm[Pk2], None}, {HoldForm[Pk1], None}},
PlotLabel -> HoldForm[c = 0.1 M时公式 Subscript[H, x3] 的可行域],
LabelStyle -> {15, GrayLevel[0]}];
cp3inf =
Table[{FindRoot[{c + 10^-(PH + 0.02) ==
kw/10^-(PH + 0.02) + c ((10^-(PH + 0.02)*10^-Pk1 + 2*10^-Pk1*10^-Pk2)/(
10^(-2 (PH + 0.02)) + 10^-(PH + 0.02)*10^-Pk1 + 10^-Pk1*10^-Pk2)),
PH == 1/2 Pk1 + 1/2 Pk2, Pk2 == a}, {Pk1, 20}, {Pk2, a}, {PH, 20},
WorkingPrecision -> MachinePrecision][[1, 2]], a}, {a, 0, 14, 0.05}];
cp3infline =
ListLinePlot[cp3inf, PlotTheme -> "Detailed", PlotStyle -> Orange,
FrameLabel -> {{HoldForm[Pk2], None}, {HoldForm[Pk1], None}},
PlotLabel -> HoldForm[c = 0.1 M时公式 Subscript[H, x3] 的可行域],
LabelStyle -> {15, GrayLevel[0]}];
Show[cp3supline, cp3infline,
Graphics[{Thick, Dashed, Orange, Line[{cp3inf[[1]], cp3sup[[1]]}]}],
AspectRatio -> 1]
|
完整可行域:
cp3infsurface =
ContourPlot3D[
10^-Pc + 10^-(1/2 Pk1 + 1/2 Pk2 + 0.02) == kw/10^-(1/2 Pk1 + 1/2 Pk2
+ 0.02) + 10^-Pc*((10^-(1/2 Pk1 + 1/2 Pk2 + 0.02)*10^-Pk1 +
2*10^-Pk1*10^-Pk2)/(10^(-2 (1/2 Pk1 + 1/2 Pk2 + 0.02)) +
10^-(1/2 Pk1 + 1/2 Pk2 + 0.02)*10^-Pk1 +
10^-Pk1*10^-Pk2)), {Pk1, -1, 20}, {Pk2, -5, 16}, {Pc, -1, 7},
ContourStyle -> {RGBColor[0.5355579515419151, 0.9430131641554946,
0.004882822085237493], Opacity[0.5]}, ImageSize -> {500, 500},
AxesLabel -> Automatic, AxesStyle -> Directive[Black, 17],
PlotLegends -> {"surface for inf"}, PlotRange -> Full,
PlotTheme -> "Scientific", Mesh -> None];
cp3supsurface =
ContourPlot3D[
10^-Pc + 10^-(1/2 Pk1 + 1/2 Pk2 - 0.02) ==
kw/10^-(1/2 Pk1 + 1/2 Pk2 - 0.02) +
10^-Pc*((10^-(1/2 Pk1 + 1/2 Pk2 - 0.02)*10^-Pk1 + 2*10^-Pk1*10^-Pk2)/
(10^(-2 (1/2 Pk1 + 1/2 Pk2 - 0.02)) + 10^-(1/2 Pk1 + 1/2 Pk2 - 0.02)
*10^-Pk1 + 10^-Pk1*10^-Pk2)), {Pk1, -1, 20}, {Pk2, -5, 16}, {Pc, -1, 7},
ContourStyle -> {RGBColor[0.5864078175768783, 0.26359194937432395`,
0.519486597936422], Opacity[0.5]}, ImageSize -> {500, 500},
AxesLabel -> Automatic, AxesStyle -> Directive[Black, 17],
PlotLegends -> {"surface for sup"}, PlotRange -> Full,
PlotTheme -> "Scientific", Mesh -> None];
shadow3inf =
Plot3D[-Log10[(kw/10^-(1/2 Pk1 + 1/2 Pk2 + 0.02) -
10^-(1/2 Pk1 + 1/2 Pk2 + 0.02))/(1 - ((10^-(1/2 Pk1 + 1/2
Pk2 + 0.02)*10^-Pk1 + 2*10^-Pk1*10^-Pk2)/(10^(-2 (1/2 Pk1 + 1/2 Pk2 + 0.02))
+ 10^-(1/2 Pk1 + 1/2 Pk2 + 0.02)*10^-Pk1 +
10^-Pk1*10^-Pk2)))], {Pk1, -1, 20}, {Pk2, -5, 16},
PlotStyle -> Directive[RGBColor[0.5355579515419151, 0.9430131641554946,
0.004882822085237493], Opacity[0]], Filling -> Bottom, Mesh -> None,
BoundaryStyle -> None];
shadow3sup =
Plot3D[-Log10[(kw/10^-(1/2 Pk1 + 1/2 Pk2 - 0.02) -
10^-(1/2 Pk1 + 1/2 Pk2 - 0.02))/(1 - ((10^-(1/2 Pk1 + 1/2 Pk2 - 0.02)
*10^-Pk1 + 2*10^-Pk1*10^-Pk2)/(
10^(-2 (1/2 Pk1 + 1/2 Pk2 - 0.02)) +
10^-(1/2 Pk1 + 1/2 Pk2 - 0.02)*10^-Pk1 +
10^-Pk1*10^-Pk2)))], {Pk1, -1, 20}, {Pk2, -5, 16},
PlotStyle -> Directive[RGBColor[0.5864078175768783, 0.26359194937432395`,
0.519486597936422], Opacity[0]], Filling -> Bottom, Mesh -> None,
BoundaryStyle -> None];
Show[cp3infsurface, cp3supsurface, shadow3inf, shadow3sup]
|